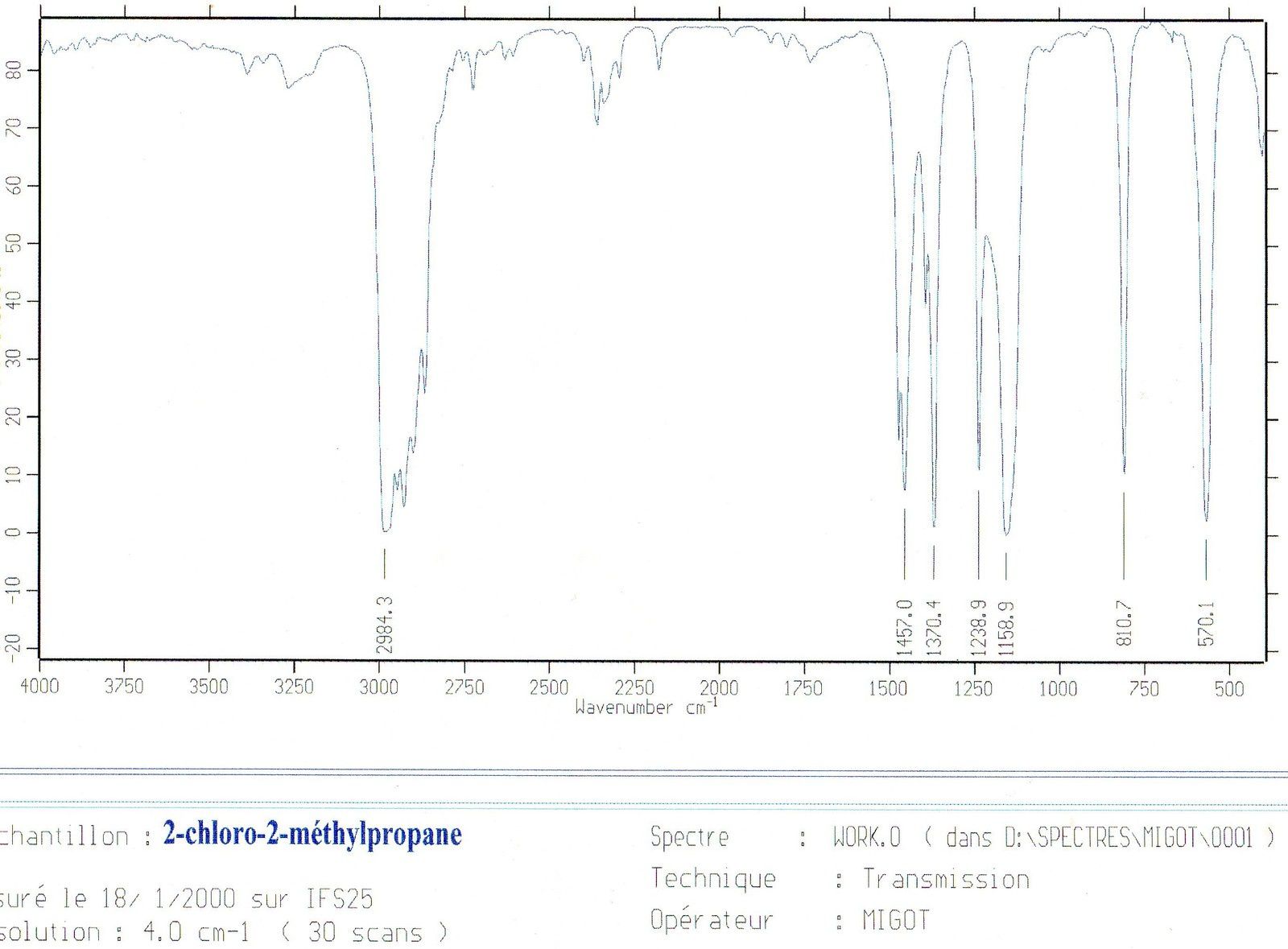
2-chloro-2-méthylpropane
(méthode de Boedtker - 1904)
(test de Lucas - 1930)
La substitution nucléophile monomoléculaire, plus couramment appelée SN1 est un mécanisme réactionnel en chimie organique.
C'est un mécanisme limite, au sens où des réactions chimiques « naturelles » usant de ce type de mécanisme ne se font jamais entièrement selon ce mécanisme, mais à un certain pourcentage.
Le mécanisme limite « opposé » est la SN2. Ces deux mécanismes sont utilisés pour décrire la réaction :
- R-GP + Nu− = R-Nu +GP−
où GP est le groupe partant (aussi appelé nucléofuge), Nu est le nucléophile, et R un radical alkyle ou aryle.
Mécanisme
La réaction se fait en deux étapes.
Le groupe partant GP réagit sur lui-même. La liaison R-GP se rompt pour donner un carbocation R+ et un ion GP−. C'est une réaction très lente et déterminante pour la cinétique de la réaction.
Exemple avec du 3-chloro-3-éthylpentane : ici c'est le groupe Cl qui joue le rôle de groupe partant. Les lobes en bleu représentent l'orbitale p vacante.
Le nucléophile Nu− réagit immédiatement (étape rapide) avec le carbocation juste après sa formation. Le nucléophile peut attaquer le carbocation, qui est de géométrie trigonale plane, en dessous ou au-dessus du plan.
Avec l'exemple précédent, le produit est le même quel que soit le côté attaqué car le 3-chloro-3-ethylpentane est une molécule achirale.